微小管の引張が促進するダイニン物質輸送
新たな細胞制御メカニズムの解明
2024年8月2日
発表ポイント
-
微小管が引張応力(引っ張り)によって変形することを発見。
-
ダイニンによる物質輸送速度は弱い引張応力下の微小管で速くなる。
-
物質輸送の促進や阻害が関与する神経疾患などの治療への貢献。
概要
京都大学大学院理学研究科の日本学術振興会特別研究員であるナスリン サエダ・ルバイヤ博士、同大学院理学研究科の角五彰教授らの研究グループは、星薬科大学薬学部、東京大学先端科学技術研究センターの山下雄史准教授、横浜市立大学大学院生命医科学研究科の池口満徳教授、国立研究開発法人情報通信研究機構(NICT)の鳥澤嵩征研究員(現 国立遺伝学研究所)と大岩和弘主管研究員と共同で、微小管に引張応力を与えた際のモータータンパク質による物質輸送速度の変化について研究を行いました。本研究は、独自開発した伸展機構を介し、微小管に定量的な引張応力を加え、ダイニンモーターによる物質輸送を観察しました。高度な蛍光顕微鏡イメージング技術と定量的に引張応力を与える技術を使用し、シリコーンゴム基板上で引張応力を微小管に加えました。一定以下の引張応力下ではダイニンの物質輸送速度の向上を示しますが、一定以上の引張応力では輸送速度が減少することが示されました。このことは微小管の変形やダイニンと微小管の相互作用の変化が輸送速度の変化を引き起こすことを示唆しています。これらの発見は、細胞内の力と分子モーターの相互作用に関する新たな知見をもたらし、細胞内物質輸送を維持する上での微小管の力学特性の重要性を浮き彫りにしています。本研究の成果は、2024年6月25日よりアメリカ化学会ACS Publicationsが発行する国際学術誌「Nano Letters」のウェブサイトにオンラインで公開されました。
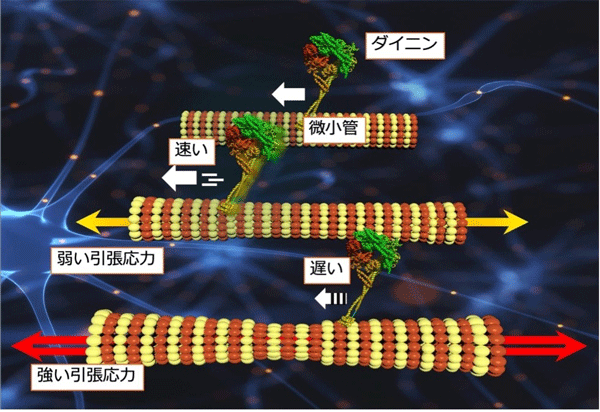
図1 微小管に引張応力を与えた際のダイニンの物質輸送速度の変化
背景
細胞骨格の一つである「微小管」は細胞の形態形成や細胞内物質輸送などにおいて重要な役割を果たしています。微小管に力学ストレスがかかることで微小管が変形することは知られているものの、変形した微小管上における細胞内物質輸送については完全には理解されていません。これまでの研究では、微小管が圧縮による力学ストレスを受けた際に、細胞内物質輸送に変化が生じることが明かされていました。一方で、微小管が引っ張りによる力学ストレスを受けた際の細胞内物質輸送の変化は不明のままであり、本研究はその解明を目的として行われました。
研究手法
本研究は、引張応力下における細胞内物質輸送の変化を調べるために、量子ドットを輸送するダイニンモータータンパク質を観察しました。この際に引張応力を定量的に与えるために、シリコーンゴム基板を介して引張応力を与えています。
結果
本研究は、ある一定の強さまで微小管に引張応力を加えられるとダイニンによる物質輸送速度が上がり、それ以上の強さの引張応力を加えると物質輸送速度が下がることを示しました。さらに、物質輸送速度に非線形性が生じる理由を解明するために、全原子分子動力学 (MD) シミュレーションを使用して、ダイニンと微小管ユニット間の相互作用エネルギーを明らかにしました。この結果、弱い引張応力による微小管の変形は、ダイニンと微小管の相互作用を弱め、輸送速度を促進することがわかりました。これは、微小管の力学特性が単に受動的ではなく、ダイニンをはじめとするモータータンパク質の機能に積極的に影響し、力が細胞内情報担体として働き、その結果、細胞内輸送ダイナミクスに影響を与えることを示唆しています。ルバイヤ博士、角五教授らは微小管の引張試験とダイニンによる物質輸送の評価、鳥澤博士、大岩博士らはダイニンの発現系の確立とその試料の供与および試験管内運動アッセイに関する助言、山下准教授、池口教授らは全原子分子動力学 (MD) シミュレーションを担当しました。
波及効果・今後の予定
本研究は、細胞内輸送メカニズムの重要な側面、具体的には、微小管への引張応力がダイニンの物質輸送に与える影響を解明しました。微小管に与えられる引張応力が細胞内物質輸送へ与える影響を理解することで、微小管への力学的ストレスを要因とする外傷性脳損傷や微小管の変形が関連するハンチントン病やパーキンソン病などの神経疾患研究への波及が期待されています。例えば、本研究が細胞内物質輸送の欠陥に由来する神経疾患の治療法開発のフレームワークとなることも期待されます。今後、研究グループは反復的に応力を加えることで微小管におよぼす影響と、その結果として微小管の機能がどのように変化するかの調査を予定しています。
研究プロジェクトについて
本研究は、京都大学研究支援・実験補助者雇用制度、文部科学省日本学術振興会科学研究費助成事業(22K18165, 18H05426, JP18H05423, JP21H04434, JP17K19211)、東京大学GAPファンドプログラム、および国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)の助成事業(JPNP20006)の助成を受けたものです。また、東京工業大学のスーパーコンピュータTSUBAME3.0を利用して実施しました。
研究者のコメント
一般に、道路に損傷があった場合には交通が妨げられます。しかし、細胞内輸送では興味深いことに、細胞内の道路である微小管が引張応力を受けると、モータータンパク質であるダイニンはより高速で物質輸送をすることを発見しました。私たちの研究は、細胞内輸送ダイナミクスにおける応力の重要な役割を明らかにしています。また、私たちの発見は、細胞内輸送の基本的メカニズムに関する新たな知見を提供します。この知見がさまざまな細胞プロセスや疾患の理解に繋がる可能性を秘めています。(ナスリン サエダ・ルバイヤ)
論文情報
タイトル:Tensile stress on microtubules facilitates the dynein-driven cargo transport
著者:Syeda Rubaiya Nasrin, Takefumi Yamashita, Mitsunori Ikeguchi, Takayuki Torisawa, Kazuhiro Oiwa, Kazuki Sada and Akira Kakugo
掲載誌:Nano Letters
用語解説
モータータンパク質
アデノシン三リン酸(ATP)の加水分解によって生じる化学エネルギーを運動に変換するタンパク質のことです。生物のほとんどすべての細胞に存在しており、物質の輸送や細胞分裂に関わっています。アクチン上を動くミオシン、微小管上を動くキネシンやダイニンが知られており、本研究では微小管とダイニンを使用しています。
全原子分子動力学 (MD) シミュレーション
原子の動きをシミュレーションする計算技術です。全原子MDシミュレーションは、系内のすべての原子を明示的にモデリングし、その相互作用を計算します。これにより、タンパク質や他の生体分子の構造やダイナミクスを詳細に解析することが可能になります。全原子MDシミュレーションは、分子レベルでの新薬設計や生物学的機能の解明において重要なツールとして広く用いられています。
研究に関する問合せ先
国立研究開発法人情報通信研究機構
未来ICT研究所
主管研究員大岩 和弘(おおいわ かずひろ)
E-mail: oiwa nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp報道に関する問合せ先
国立研究開発法人情報通信研究機構
広報部 報道室
E-mail: publicity nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp