バイオナノマシンの運動性の基本原理を実証
——定説の運動機構を覆しうる発見——
2024年7月22日
発表のポイント
-
バイオナノマシン・キネシンの一方向力発生の根源となる運動性の計測に成功しました。
-
DNAナノテクノロジーを用い、キネシンのモータードメイン内のループ領域に運動支点を自在にデザインする手法を開発しました。
-
生体高分子の運動の基幹機構を理解することで、人工マシンとは異なる原理で動作する生体素材からつくるバイオナノロボットの設計指針を得られることが期待されます。
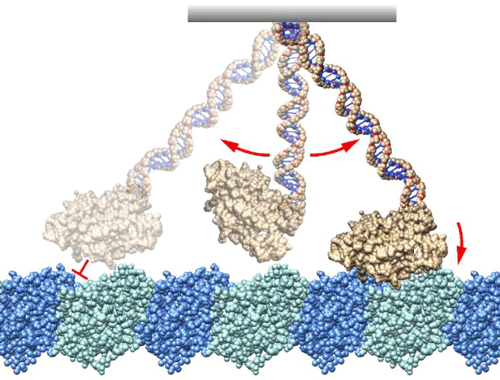
外部負荷方向によって運動方向が制御されるキネシンの運動性起源の検出に成功
概要
東京大学大学院総合文化研究科広域科学専攻の住吉里英子大学院生、山岸雅彦助教、矢島潤一郎教授、学習院大学の西坂崇之教授、国立研究開発法人情報通信研究機構(NICT)未来ICT研究所の古田茜研究員、古田健也研究マネージャーらは、バイオナノマシンの一種、キネシンのモータードメインを構成するループ領域に微小なDNAオリゴマーを結合させ、自在に運動支点をデザインする方法を開発し、どのような運動支点であってもキネシンは、細胞骨格・微小管に作用して一方向に力を発生できることを明らかにしました。従来は、モータードメインとテイルドメインを繋ぐリンカードメインの構造変化が力発生の起源と考えられていましたが、本研究により従来モデルを大きく修正する必要が生じました(図1)。バイオナノマシンは、人間が作るマシンとどことなく似ているように捉えることもできますが、運動する仕組みは似て非なるものです。本研究成果は、生体高分子から構成されるミクロなバイオナノロボットを設計するための指針を与えるものとして期待できます。
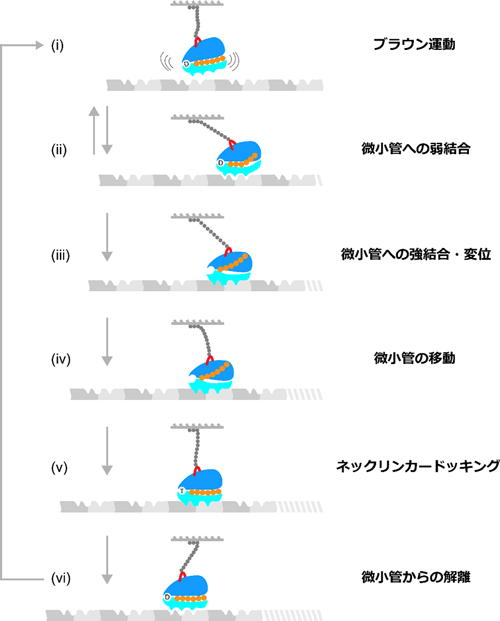
図1:バイオナノマシン・キネシンの運動モデル
キネシンモータードメイン(青)のループ領域(赤)を運動支点とした運動モデル。ADP(D)が結合したモータードメインが微小管レール(灰色)と結合することで、モータードメイン内の運動支点となったループ部位に特定方向への外部負荷がかかると、モータードメインが微小管と強結合状態に遷移し力発生をする。ATP(T)の結合したモーターコアへのネックリンカー(オレンジ)のドッキングによって、モータードメインと微小管との結合や解離が調節される。
発表内容
我々の体を構成する細胞の中では、所狭しと10ナノメートル(1ミリメートルの十万分の1)程の大きさのタンパク質からなるバイオナノマシンが働いています。染色体分配、細胞質分裂、細胞内小胞輸送等において力仕事を担うバイオナノマシン・キネシンやダイニンは、細胞骨格の一種である微小管上を運動することがよく知られています。キネシンの運動モデルとして、「ネックリンカードッキングモデル」が世界で流布しています。このモデルでは、ネックリンカーと呼ばれるモータードメインの末端の15アミノ酸程度の領域が大きく構造を変え、このネックリンカーの構造変化が運動発生の実体であり、ちょうど人間が足首を曲げることで前方に移動することと類似するため直観的にわかりやすい運動モデルでした。しかしながら、これまでの先行研究では、ネックリンカーが運動に直接関わらない条件下でキネシンの運動を計測した報告はなく、ネックリンカーの構造変化とキネシンの運動の関係性は明確ではありませんでした。
この度、本研究グループはキネシンの運動を生じる最小構成単位であるモータードメインのあらゆる部位に対して微小な二重鎖DNAを結合させる手法を開発し、結合したDNAの逆末端を基板に固定することでモータードメインの運動支点を自在に設定し、このモータードメインによって駆動される微小管の運動を計測しました(図2)。モータードメイン内の運動支点となるアミノ酸に点変異を導入するだけでDNAオリゴマーを結合できるため、キネシンの運動能への影響を最小限に抑えられるうえ、DNAの塩基長を調節することで固定基板とモータードメインの間隔を確保してモータードメインの自由度を保ち、従来では困難であったネックリンカーが物理的に運動にかかわらない状態で運動計測を可能としました。
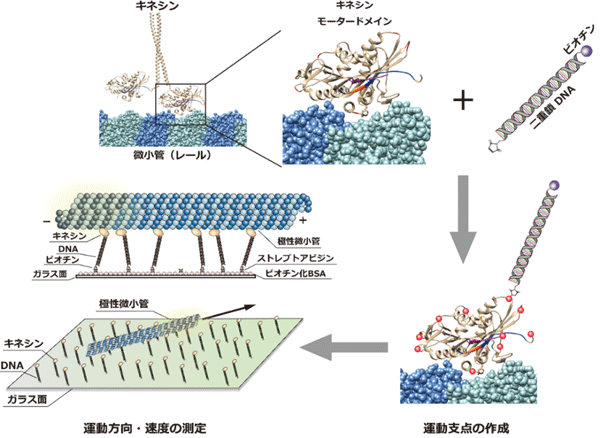
図2:モータードメイン内のループ領域を運動支点として運動性を定量する方法
モータードメインの特定アミノ酸に対してシステイン-マレイミド結合を用いて二重鎖DNAを結合し、ガラス基板面にDNAを介してキネシンを固定することで、従来法のネックリンカー以外のループ領域を運動支点とした。キネシンが極性微小管を移動させる様子を計測し、運動支点に依存したキネシンの運動方向、及び、運動速度を定量した。
それぞれの運動支点で固定したキネシンに駆動される微小管のイメージング画像から、運動方向や運動速度を定量した結果(図3)、どのループ位置に運動支点を設定したとしても、モータードメインによって駆動される運動が計測され、ネックリンカーの動きが物理的に運動に直接関与していなくてもキネシンが運動できること、すなわち、運動を生じさせる実体がネックリンカーの構造変化とは別に存在することが示されました。さらに、その運動方向は、これまで報告されていた順行性方向だけではなく、逆行性方向の運動性を示す支点位置が幾つか検出され、キネシンのモータードメインは元来一方向運動性を有していたわけではなく、両方向性を保持し、進化の過程で一方向運動性を獲得した可能性が示唆されました。
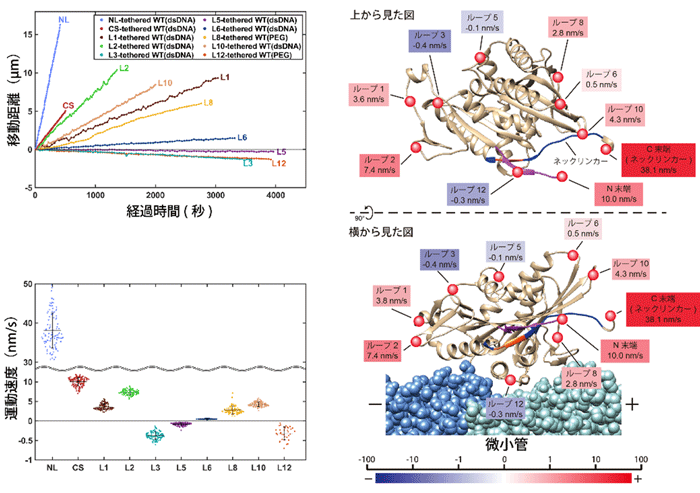
図3:キネシンモータードメイン内の運動支点による運動方向、及び、運動速度
モータードメイン(茶)内にデザインした運動支点(オレンジ)それぞれの場合の運動方向・速度を計測した。ループ3、ループ5、ループ12を運動支点とした場合には、キネシンの通常の運動方向とは逆の逆行性モーターの性質を示した。
さらに構造データの解析から、ATP結合に伴うループ領域の微小管の長軸に沿った方向の構造変化は僅か数Å程度で、ネックリンカーの構造変化距離(数十Å)に比して小さく、構造変化の方向も運動方向と一致しないことがわかりました(図4)。こうしたネックリンカーの構造変化が一方向性運動発生の主体であるとする従来モデルでは説明できないような本研究の結果に基づき、ブラウニアンラチェット理論も踏まえ、モータードメインが微小管の前・後方向に対して結合、及び、解離する度合いが、モータードメイン内の支点部位にかかる負荷方向によって運動方向を制御するという運動モデルを提唱しました(図1)。
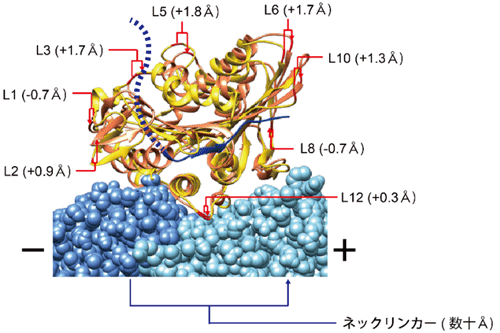
図4:キネシンモータードメイン内の各ループ領域の構造変化
ATP結合前(黄)とATP結合後(オレンジ)のモータードメイン構造の重ね合わせ。運動支点として設定したループ領域付近の構造変化はいずれも数Åに留まり、ネックリンカー(青)の構造変化(数十Å)に比べて非常に小さいうえ、構造変化の方向と運動方向も一致していない。
今後の展開
本研究では、キネシンのモータードメイン内のループ位置を運動支点とし、ネックリンカーの構造変化自体が直接動きに変換されない条件でもキネシンが運動できるという、従来の定説を覆しうる新たな知見を提供しました。さらに、モータードメインが両方向運動性を有すことを見出し、モータードメインにかかる外部負荷状況に応じて運動方向が決定されている可能性も示しました。しかしながら、モータードメインと微小管との結合と解離の両方、もしくは、どちらか一方のみが変調されて一方向運動性が生じているのかどうかといった運動が創発される実体が実験的に示されていないため、運動の基幹機構の解明に迫るさらなる研究が必要です。バイオナノマシンに特徴的な確率過程が含まれる運動機構を解明することによって、人工マシンとは異なる原理で動作するバイオミメティック(生体模倣的)な発動分子マシンの創製の設計指針になることが期待されます。
関連情報
- 「プレスリリース①バイオナノマシンチームの螺旋運動の分子機構に迫る——バイオナノロボの設計に向けて——」(2022/12/20)
https://www.u-tokyo.ac.jp/focus/ja/press/z0109_00071.html - 「プレスリリース②バイオナノマシンの運動の左右対称性を破る分子機構に迫る~ミクロな発動分子マシンの設計に向けて~」(2021/2/10)
https://www.u-tokyo.ac.jp/focus/ja/press/z0109_00008.html
発表者・研究者等情報
東京大学大学院総合文化研究科 広域科学専攻
住吉 里英子 博士課程/日本学術振興会特別研究員
山岸 雅彦 助教
矢島 潤一郎 教授
国立研究開発法人情報通信研究機構
未来ICT研究所 神戸フロンティア研究センター バイオICT研究室
古田 茜 研究員
古田 健也 研究マネージャー
学習院大学理学部
西坂 崇之 教授
University of Warwick, Warwick Medical School
Robert A. Cross(ロバート・クロス) 教授
論文情報
雑誌名:Proceedings of the National Academy of Sciences
題名:Tether-scanning the kinesin motor domain reveals a core mechanical action
著者名:Rieko Sumiyoshi*, Masahiko Yamagishi*, Akane Furuta, Takayuki Nishizaka, Ken'ya Furuta, Robert A. Cross, Junichiro Yajima
DOI: 10.1073/pnas.2403739121
研究助成
本研究は、科研費「基盤C(課題番号:JP15K07022)」、「挑戦的萌芽(課題番号:JP23K18135)」、「若手研究(課題番号:JP23K14177)」「学術変革(課題番号:JP21H00386)」「学術変革(課題番号:JP23H04401)」、「特別研究員奨励費(課題番号:JP23KJ0813)」、及びWellcome Investigator Award (220387/Z/20/Z)の支援により実施されました。深く感謝いたします。
用語解説
バイオナノマシン
細胞内には力仕事を行うタンパク質が存在します。細胞骨格・微小管と相互作用するバイオナノマシンとしては、モータータンパク質「キネシン」や「ダイニン」が、細胞骨格・アクチンと相互作用するバイオナノマシンとしてはモータータンパク質「ミオシン」がよく知られています。ATPなどの化学物質の加水分解エネルギーを利用して力学的仕事を行う。本研究では、キネシンを用いました。
キネシン
バイオナノマシンの一種でリニアモータータンパク質に分類されます。細胞内の様々な力学的現象に関わり、真核細胞に必須のタンパク質です。ATPの加水分解エネルギーを力学的仕事に変換するタンパク質であることが特徴的です。
細胞骨格
細胞内でタンパク質繊維のネットワークを形成し、細胞の形態維持、細胞内輸送等に構造タンパク質として関わるとともに、細胞運動、細胞分裂等に力を発生するバイオマシンとしても関わり、細胞現象に重要な役割を果たします。真核生物では、微小管、アクチンフィラメント、中間径フィラメントが主要な細胞骨格として存在し、本研究では微小管を用いました。
ブラウニアンラチェット理論
微小粒子が溶液中で他の分子からの衝突で揺らぐ現象をブラウン運動といいます。ブラウン運動の方向はランダムですが、このランダム運動から一方向性運動を取り出す理論です。
研究内容に関する問合せ先
東京大学
大学院総合文化研究科 広域科学専攻
教授 矢島 潤一郎(やじま じゅんいちろう)Tel:03-5454-6745
E-mail: yajima bio.c.u-tokyo.ac.jp
bio.c.u-tokyo.ac.jp
 bio.c.u-tokyo.ac.jp
bio.c.u-tokyo.ac.jp
国立研究開発法人情報通信研究機構
未来ICT研究所 神戸フロンティア研究センター
バイオICT研究室
研究マネージャー 古田 健也(ふるた けんや)
E-mail: furutak nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp広報
東京大学
大学院総合文化研究科 広報室
Tel:03-5454-6306
E-mail: pro-www.c gs.mail.u-tokyo.ac.jp
gs.mail.u-tokyo.ac.jp
 gs.mail.u-tokyo.ac.jp
gs.mail.u-tokyo.ac.jp
国立研究開発法人情報通信研究機構
広報部 報道室
E-mail: publicity nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp